Wat is een systematische review en wat leer je in dit leerpad?
Systematische reviews verzamelen bewijsmateriaal dat voldoet aan vooraf vastgestelde inclusiecriteria, met als doel een specifieke onderzoeksvraag te beantwoorden. Ze streven ernaar bias te minimaliseren door gebruik te maken van expliciete, systematische methoden die vooraf in een protocol worden vastgelegd. (vertaling van Cochrane handbook)
Onderstaand leerpad is opgebouwd volgens de stappen die je dient te doorlopen bij het maken, publiceren en bekend maken van je systematische review.
Stap 1: de literatuur verkennen en planning
Je leert waarom het verkennen van de beschikbare literatuur essentieel is vóór je aan een systematische review begint. Je leert hoe deze zoektocht helpt om je onderzoeksvraag en selectiecriteria aan te scherpen. Verder leer je het belang van de verkennende zoekopdracht om op basis van je bevindingen de relevantie, haalbaarheid en planning van je review te onderbouwen.
Een verkenning van de beschikbare literatuur helpt op verschillende manieren:
- om je onderzoeksvraag scherp te stellen;
- je selectiecriteria verder af te bakenen (zie stap 3 en stap 5);
- de relevantie van je review te bevestigen;
- articles te identificeren die later belangrijk zullen zijn om je zoekstrategie op te stellen;
- het geeft je een eerste indruk van de omvang en de aard van de gepubliceerde studies.
Deze voorbereidende stap is essentieel voordat je effectief start met een systematische review. Op basis van je bevindingen uit deze verkennende stap, bepaal je of je oorspronkelijke onderzoeksdoel uitvoerbaar en gepast is voor een systematische review. Hierdoor kan je ofwel je onderzoeksdoel en onderzoeksvraag scherp stellen of bekijken of je niet beter overschakelt naar een andere type review. Voor een systematische review verbind je je er namelijk toe om alle evidence te identificeren. Het is daarom aangeraden om voor een systematische review verder te gaan met een specifieke en welomlijnde onderzoeksvraag. Is het doel van je onderzoek om een breed overzicht te geven van welke informatie er beschikbaar is in de literatuur? Dan raden we aan om je type review aan te passen (naar bijv. een scoping review).
Gebruik deze zoektocht om key articles te vinden die je later zullen helpen om je definitieve zoekstrategie op te stellen.
Gebruik deze zoektocht ook om te bevestigen dat het doel van je onderzoek en de onderzoeksvraag is aangepast aan het type review, of pas het type review aan aan het doel van je onderzoek.
Bij deze stap heb je vooral een databank nodig die het beste aansluit bij jouw onderwerp. Gebruik hiervoor de KCGG databanken-pagina waar de inhoud van de databank dient als leidraad. Voor een verkenning van de (bio)medische literatuur is MEDLINE (bijvoorbeeld via PubMed of Ovid) doorgaans een goed startpunt. Heb je een farmacologische vraag? Dan is Embase (bij UGent via embase.com) vaak geschikter. Bij een onderwerp rond verpleegkunde en paramedische onderwerpen kan je kiezen voor CINAHL (bij UGent via EBSCO).
Voordat je start met je review over de effectiviteit van een nieuw geneesmiddel, voer je een snelle zoektocht uit in de databank Embase om te zien of er al vergelijkbare reviews zijn en om key articles te vinden.
- KCGG databanken-pagina: https://www.kcgg.ugent.be/zoeken/databanken/
- Blits-informatiesessie: Hoe kies je jouw reviewtype (Nederlandstalig) / How to choose your review type (English)
- Volgende relevante vragen op de KCGG-website: https://www.kcgg.ugent.be/zoeken/zoekstrategie/
- Welk type review kies ik best? Om kritisch een keuze te maken rond het uitvoeren van een systematische review of eerder een ander type review.
- Waar vind ik systematische reviews? Om te zoeken naar andere vergelijkbare reviews (secundaire studies), naast het zoeken van (primaire) studies die je zal includeren in jouw review.
- Volgende relevante vragen op de KCGG-website: https://www.kcgg.ugent.be/zoeken/zoekstrategie/
Stel jezelf op basis van deze verkennende stap de volgende vragen:
- Zijn er al recente systematische reviews over dit onderwerp? Zo ja, welke onbeantwoorde vragen of hiaten in de kennis (of ‘knowledge gaps’) kan mijn geplande review opvullen?
- Is de hoeveelheid literatuur hanteerbaar of overweldigend?
- Is er een voldoende aantal geschikte studies beschikbaar die de specifieke populatie of interventie onderzoeken die ik wil bestuderen?
- Wat is de algemene aard van de beschikbare studies? Zijn ze methodologisch vergelijkbaar (homogeen) qua opzet, populatie en interventie, of vertonen ze juist aanzienlijke verschillen (heterogeen)?
- Zijn de resultaten van de studies geschikt om te combineren voor een kwantitatieve synthese, bijvoorbeeld een meta-analyse? Of is er sprake van aanzienlijke variatie tussen de studies, wat een kwantitatieve synthese minder passend maakt?
- Is het realistisch om de gehele systematische review uit te voeren, inclusief de verplichting om alle relevante evidence te identificeren, op kwaliteit te beoordelen en te synthetiseren?
- Is mijn onderzoeksvraag het meest geschikt voor een systematische review, of zou een ander type review, zoals een scoping review, beter aansluiten bij het doel?


Stap 2: Richtlijnen ter ondersteuning bij het uitvoeren van systematische reviews
In deze stap leer je welke methodologische richtlijnen (guidelines for conducting) beschikbaar zijn om je te ondersteunen bij het opzetten en uitvoeren van systematische reviews. Je leert hoe je op basis van je onderzoeksvraag, het type review en het soort data kiest welke richtlijn geschikt is. Verder leer je hoe je op basis van deze richtlijn je methodologie onderbouwt en argumenteert in functie van de relevantie, haalbaarheid en planning van je review.
Methodologische richtlijnen helpen je om je systematische review op een transparante, reproduceerbare en kwaliteitsvolle manier op te zetten en uit te voeren. Afhankelijk van het type review (bijvoorbeeld interventie of diagnostiek) bestaan er specifieke richtlijnen met aangepaste stappen.
Let op: het gaat hier om conducting guidelines, richtlijnen om de systematische review uit te voeren. Deze verschillen fundamenteel van reporting guidelines zoals PRISMA. Reporting guidelines komen van pas om je uitgevoerde systematische review te rapporteren. Deze reporting guidelines komen aan bod in stap 16 (Rapporteren).
Een correcte keuze van conducting guideline verhoogt ook de kans dat je review rigoureus, transparant en (internationaal) bruikbaar is.
Richtlijnen die je kan gebruiken staan onder ‘Tools’ in dit hoofdstuk.
Gebruik enerzijds een conducting guideline om je review op te zetten en uit te voeren en anderzijds een reporting guideline om je review te rapporteren (zie stap 16). PRISMA is géén richtlijn voor het opzetten en uitvoeren van je review.
Denk na over heterogeniteit: de mate van heterogeniteit (bv. populaties, interventies, uitkomstmaten) kan mee bepalen welke methode of guideline geschikt is, en of een narratieve synthese of meta-analyse aangewezen is.
Gebruik de guideline niet pas achteraf: integreer de aanbevelingen vanaf het begin van je protocolfase (zie stap 3).
Verduidelijk je keuze: geef in je protocol en methodesectie aan welke richtlijn je gebruikt en waarom.
Alle Cochrane-reviews volgen de richtlijnen uit het Cochrane Handbook. Voorbeelden van dergelijke reviews vind je in de Cochrane Database of Systematic Reviews (CDSR) via de Cochrane Library: https://www.cochranelibrary.com/cdsr/reviews.
Het is aanbevolen om binnen deze databank een review te raadplegen uit je eigen discipline. Zo zie je meteen hoe de richtlijnen in de praktijk worden toegepast in een context die voor jouw vakgebied relevant is.
- Specialist course ‘Conducting and publishing a systematic review and meta-analysis’ van het KCGG: https://ufora.ugent.be/d2l/le/discovery/view/course/79669
- Cochrane Handbook for Systematic Reviews of Interventions: training.cochrane.org/handbook
- Cochrane Handbook for Systematic Reviews of Diagnostic Test Accuracy: https://training.cochrane.org/handbook-diagnostic-test-accuracy/current
- Methodological articles published by PERSyst (Prevalence Estimates Reviews – Systematic Review Methodology Group): https://persyst.group/
- Conducting guideline for Systematic Reviews of Outcome Measurement Instruments van COSMIN: https://www.cosmin.nl/tools/guideline-conducting-systematic-review-outcome-measures/
- JBI manual for evidence synthesis: https://jbi-global-wiki.refined.site/space/MANUAL
Stel jezelf op basis van deze stap de volgende vragen:
- Heb ik een weloverwogen keuze gemaakt voor de meest geschikte conducting guideline voor mijn specifieke onderzoeksvraag en type review? Welke factoren waren doorslaggevend voor deze keuze?
- Begrijp ik het fundamentele verschil tussen een conducting guideline (voor het uitvoeren) en een reporting guideline (voor het rapporteren)?
- Weet ik hoe ik de gekozen guideline moet integreren in de protocolfase (Stap 3) van mijn review, in plaats van deze pas achteraf te raadplegen?
- Kan ik argumenteren waarom deze specifieke guideline het meest geschikt is voor mijn review en hoe deze bijdraagt aan de robuustheid en transparantie van mijn onderzoek?
Stap 3: protocol opstellen
- Waarom een protocol cruciaal is voor transparantie en reproduceerbaarheid.
- Welke onderdelen minimaal in een protocol moeten opgenomen worden.
- Waarom je zo vroeg in je traject met het opstellen van je protocol dient te starten.
Een protocol is het plan voor je review. Het omvat je onderzoeksvraag en doelstelling, je inclusie- en exclusiecriteria, je zoekstrategie, je selectieprocedure, je data-extractieplan, je kwaliteits- of biasbeoordeling, je analyse- en syntheseplan, je tijdslijn en de rolverdeling. Volg voor het opstellen de PRISMA-P richtlijnen, die aangeven welke onderwerpen minimaal in je protocol dienen opgenomen te worden en op welke manier. Het beschikbaar stellen van je protocol zorgt voor transparantie, voorkomt dat anderen onbedoeld dezelfde review uitvoeren en helpt bias te verminderen (zie Stap 8: protocol registreren en/of publiceren).
Zorg dat alle relevante teamleden (bijv. promotor, begeleider, 2de reviewer, ev. statisticus, ev. KCGG informatiedeskundige) betrokken zijn bij het opstellen van het protocol en vraag actief om hun feedback. Op die manier is er geschreven consensus over je onderwerp en methode. Als je feedback wenst voor je protocol van een informatiedeskundige van het KCGG, dan kan je dit vragen via ons formulier.
Start heel vroeg bij het uitwerken van je systematische review aan je protocol, maar finaliseer en registreer je protocol (zie Stap 8: protocol registreren en/of publiceren) bij voorkeur na je verkennende zoekopdracht, maar ten laatste voordat je start aan je data-extractie. Enerzijds zal je na je verkennende zoekopdracht een beter zicht hebben op de beschikbare literatuur, de haalbaarheid en de relevantie van je onderzoeksvraag. Anderzijds doe je dit voor de data-extractie omdat je vooraf vastlegt wat je precies gaat doen, zodat je latere keuzes niet beïnvloed worden door de resultaten in je data-extractie die je al gezien hebt.
PROSPERO en Open Science Framework (OSF) zijn platformen voor registratie van je protocol (zie meer info in stap 8: protocol registreren en/of publiceren). Op deze platformen kan je verifiëren of je onderzoekvraag uniek is en kan je inspirerende voorbeelden in jouw onderzoeksdomein vinden.
Rammant, E. et al. Rehabilitation interventions to improve patient-reported outcomes and physical fitness in survivors of muscle invasive bladder cancer: a systematic review protocol. Protocol gepubliceerd in BMJ open (doi.org/10.1136/bmjopen-2017-016054) en geregisreerd op PROSPERO: https://www.crd.york.ac.uk/PROSPERO/view/CRD42017055306
- PRISMA-P checklist (Preferred Reporting Items for Systematic Review and Meta-Analysis Protocols) bevat aanbevolen items voor een systematisch reviewprotocol
- Cochrane Handbook for Systematic Reviews of Interventions – Chapter 1 – Sectie 1.5: Protocol development
Stel jezelf op basis van deze stap de volgende vraag: “Heb ik alle onderwerpen van de PRISMA-P checklist opgenomen in mijn protocol?”


Stap 4: Je onderzoeksvraag formuleren
Je leert waarom een goed geformuleerde onderzoeksvraag de basis is van elke systematische review. Je maakt kennis met de belangrijkste frameworks die je helpen om je vraag specifiek, meetbaar, acceptabel, relevant en tijdgebonden (SMART) te maken. Verder leer je hoe je onderzoeksvraag het type review bepaalt en welke impact dit heeft op je zoekstrategie en inclusiecriteria.
Je onderzoeksvraag is het kompas van je systematische review. Een duidelijke, goed afgebakende vraag is essentieel om:
- De omvang van je review te bepalen.
- Je inclusie- en exclusiecriteria scherp te stellen.
- Een effectieve en reproduceerbare zoekstrategie te ontwikkelen.
- De methodologie van je review te onderbouwen.
- Relevantie en haalbaarheid te garanderen.
Het formuleren van een specifieke onderzoeksvraag helpt je om je te focussen op de literatuur die écht relevant is voor je doel. Een te brede vraag kan leiden tot een overweldigende hoeveelheid literatuur, terwijl een te nauwe vraag mogelijk belangrijke studies mist of niet relevant is. Waarom het zo belangrijk is om je type review af te stemmen op je onderzoeksvraag en vice versa, leer je in onze Blits-informatiesessie ‘Hoe kies je je reviewtype’ en of een ander reviewtype eventueel beter geschikt is voor jouw onderzoeksvraag.
Een framework die vooral voor systematische reviews met een klinische interventievraag worden gebruikt is PICO. Dit framework is een hulpmiddel om alle essentiële componenten van je vraag te definiëren:
- Population/Patiënt/Probleem: wie of wat wordt bestudeerd?
- Intervention: wat is de interventie of blootstelling die wordt onderzocht?
- Comparison: waarmee wordt de interventie vergeleken (bijvoorbeeld placebo, andere behandeling, geen interventie)?
- Outcome: welke uitkomst(en) worden gemeten?
Afgeleide vormen van PICO zoals PICOT (inclusief Time) en/of PICOS (inclusief Setting) bevatten meer informatie dan de klassieke PICO en zijn om die reden mogelijk een beter alternatief. Hier vind je een template voor het opstellen van PICOT vragen.
Andere frameworks kunnen relevant zijn voor andere type vragen of reviews:
- PCC (Population, Concept, Context) voornamelijk voor Scoping Reviews.
- SPIDER (Sample, Phenomenon of Interest, Design, Evaluation, Research type) voornamelijk voor kwalitatieve onderzoeksvragen.
- SPICE (Setting, Population, Intervention, Comparison, Evaluation).
- ECLIPSe (Expectation, Client group, Location, Impact, Professionals, Service).
- Wees specifiek, maar niet te beperkt. Je vraag moet namelijk voldoende afgebakend zijn om hanteerbaar te blijven, maar ook breed genoeg om alle relevante studies te omvatten. Een veelvoorkomende fout is een te brede vraag die leidt tot een overweldigende hoeveelheid en grote variëteit aan data.
- Gebruik een framework. Maak consistent gebruik van een framework (zoals PICO) om ervoor te zorgen dat alle elementen van je onderzoeksvraag duidelijk zijn.
Kan je niet alle elementen van een framework invullen? Dan is je onderzoeksvraag hoogstwaarschijnlijk te breed, te vaag én dus niet geschikt voor een systematische review. - Controleer op bestaande reviews (zie stap 1) en review protocols. Voordat je de definitieve onderzoeksvraag formuleert, controleer opnieuw of er al recente systematische reviews zijn over hetzelfde onderwerp. Als er al een review bestaat, overweeg dan om een (ander) hiaat in de literatuur aan te pakken (bijvoorbeeld een andere populatie, interventie, of uitkomst). Ga in PROSPERO na of er gelijkaardige plannen gemaakt worden binnen de onderzoeksgemeenschap.
- Overleg met je team. Bespreek je onderzoeksvraag grondig met het team. Verschillende perspectieven kunnen helpen om de vraag aan te scherpen en potentiële valkuilen te identificeren.
- Link je vraag aan je reviewtype. Zorg ervoor dat je onderzoeksvraag past bij het type systematische review dat je wilt uitvoeren (bijv. een review over de effectiviteit van een interventie versus een review over diagnostische nauwkeurigheid).
- PICO(S) framework: dit framework is een onmisbaar hulpmiddel bij deze stap.
- PICO Question Generator Tools: sommige online tools kunnen helpen bij het structureren van PICO-vragen, al zijn deze vaak eenvoudig en dien je de inhoud zelf in te vullen. Een voorbeeld hiervan: https://picotquestion.com/.
- Thesauri en woordenboeken: Gebruik medische thesauri zoals MeSH (Medical Subject Headings) van PubMed, EMTREE van Embase, of het ‘controlled vocabulary’ van CINAHL om je concepten te verduidelijken en geschikte zoektermen te vinden die passen bij je geformuleerde vraag. Bekijk ook zeker de synoniemen en/of Entry termen (of alternatieve benamingen) die beschikbaar zijn van een indexterm. Voor uitgebreide informatie rond dit deel kan je onze sessies rond de databanken bekijken via Ufora (zie kolom ‘KCGG materiaal’).
In plaats van een brede vraag als “Zijn antidepressiva effectief?”, formuleer je een specifieke vraag zoals “Zijn selective serotonin reuptake inhibitors (SSRI’s) effectiever dan tricyclische antidepressiva voor de behandeling van ernstige depressieve stoornis bij adolescenten?”
Zorg ervoor dat je elk concept voldoende helder definieert en afbakent. Denk bij de populatie bijvoorbeeld niet alleen aan termen als ‘kinderen’ of ‘adolescenten’, maar specificeer ook welke leeftijdscategorie je precies bedoelt. Een duidelijke aflijning helpt niet alleen om een gerichte en effectieve zoekstrategie op te stellen, maar ook om de juiste studies te selecteren tijdens de screeningsfase.
- https://www.kcgg.ugent.be/zoeken/zoekstrategie/ > Hoe stel ik een onderzoeksvraag op?
- Cochrane Handbook for Systematic Reviews of Interventions – Chapter 2: Determining the scope of the review and the questions it will address. Dit hoofdstuk gaat dieper in op het belang en de methoden van het formuleren van onderzoeksvragen.
Stel jezelf op basis van deze stap de volgende vragen:
- Is mijn onderzoeksvraag duidelijk en ondubbelzinnig? Kan iemand anders begrijpen wat ik wil onderzoeken?
- Heb ik een passend framework (bijv. PICO) gebruikt om mijn vraag te structureren? En zijn alle componenten van dit framework helder gedefinieerd?
- Is mijn onderzoeksvraag specifiek genoeg om een gerichte zoekstrategie te ontwikkelen, maar niet te nauw zodat belangrijke studies worden gemist?
- Is het haalbaar om deze onderzoeksvraag te beantwoorden binnen de beschikbare tijd en middelen?
- Sluit mijn onderzoeksvraag aan bij het type review dat ik van plan ben uit te voeren (bijv. een interventiereview, een diagnostische review, een prevalentie review)?
Stap 5: Je selectiecriteria opstellen
Je leert hoe je selectiecriteria (ook wel inclusie- en exclusiecriteria genoemd) opstelt. Dit zijn de specifieke kenmerken waaraan studies moeten voldoen om in je systematische review te worden opgenomen of juist te worden uitgesloten. Je leert hoe je deze criteria nauwkeurig definieert aan de hand van je eerder geformuleerde onderzoeksvraag (bijvoorbeeld je PICO-elementen), aangevuld met specifieke details over studietypes, publicatiedatum, taal en geografische regio.
Je selectiecriteria zijn de specifieke kenmerken die studies moeten bezitten om te worden opgenomen in je systematische review. Deze criteria zijn van belangrijk voor de transparantie en reproduceerbaarheid van je systematische review. Met deze criteria waak je erover dat je alleen studies die aan al je inclusiecriteria voldoen, worden opgenomen, terwijl studies die aan één of meer exclusiecriteria voldoen, worden geweerd. Deze criteria helpen je om:
- De omvang van je review verder af te bakenen.
- Objectiviteit te waarborgen tijdens het selectieproces van studies.
- De homogeniteit van de opgenomen studies te vergroten, wat belangrijk kan zijn voor bijvoorbeeld een meta-analyse.
- De zoekstrategie te verfijnen.
Definieer je criteria aan de hand van je onderzoeksvraag in framework zoals PICO (zie stap 4), aangevuld met specificities over de studietypes die je zal opnemen in je review. Bij een systematische review zijn dit uitsluitend primaire studies (dus geen reviews!). Ook limieten op vlak van publicatiedatum, taal en geografische regio horen in deze sectie. Geef ook aan indien er niet gelimiteerd wordt en indien wel, geef aan waarom (nl. rationale).
- Wees helder. Formuleer je criteria zo specifiek en objectief mogelijk, zodat twee onafhankelijke onderzoekers tot dezelfde conclusie komen over de inclusie of exclusie van een studie. Vage formuleringen (“relevante studies”) leiden tot inconsistentie.
- PICO als leidraad. Gebruik je PICO(S) elementen om de kern van je selectiecriteria te vormen. Dit zorgt voor consistentie tussen je vraag en je selectie.
- Rationale voor beperkingen. Als je limieten oplegt (bijv. op publicatiedatum of taal), motiveer dan altijd waarom dit nodig of wenselijk is. Bijvoorbeeld: “alleen Engelstalige publicaties omwille van middelenbeperkingen” of “studies na 2015 om de meest recente technieken te weerspiegelen”. Dit verhoogt de transparantie.
- Test je criteria (bij voorkeur door beide reviewers). Voordat je met de daadwerkelijke selectie begint, test je criteria op een kleine subset van studies om te zien of ze consistent kunnen worden toegepast. Pas ze indien nodig aan.
- Niet te veel, niet te weinig. Te veel exclusiecriteria kunnen leiden tot het onterecht uitsluiten van relevante studies, terwijl te weinig criteria kan resulteren in een te brede en onbeheersbare selectie. Vind de juiste balans, maar transparantie is essentieel.
Voorbeeld van selectiecriteria voor een review over “Zijn SSRI’s effectiever dan tricyclische antidepressiva voor de behandeling van ernstige depressieve stoornis bij adolescenten?”, zou je je selectiecriteria als volgt kunnen specificeren:
- Populatie: adolescenten (13-18 jaar) gediagnosticeerd met een ernstige depressieve stoornis (major depressive disorder), zoals vastgesteld met een gevalideerd diagnostisch instrument (bijv. DSM-5 of ICD-10 criteria).
- Interventie: selectieve serotonineheropnameremmers (SSRI’s) als monotherapie of in combinatie met placebo/routinezorg.
- Vergelijking: tricyclische antidepressiva (TCA’s) als monotherapie of in combinatie met placebo/routinezorg, of geen behandeling/placebo.
- Uitkomst: vermindering van depressieve symptomen, gemeten met een gevalideerde depressieschaal (bijv. Hamilton Depression Rating Scale (HAM-D) of Children’s Depression Rating Scale-Revised (CDRS-R)).
- Studieontwerp: uitsluitend gerandomiseerde gecontroleerde studies (RCT’s). Reviews, case reports, opinion papers en niet-gecontroleerde studies worden uitgesloten.
- Taal: alleen Engelstalige publicaties (rationale: middelenbeperkingen voor vertaling).
- Publicatiedatum: geen beperking op publicatiedatum (rationale: om een zo breed mogelijk overzicht van beschikbare evidentie te verkrijgen).
- https://www.kcgg.ugent.be/zoeken/zoekstrategie/ > Hoe stel ik selectiecriteria op?
- Cochrane Handbook for Systematic Reviews of Interventions – Chapter 3: Defining the criteria for including studies and how they will be grouped for the synthesis. Dit hoofdstuk biedt diepgaande richtlijnen over het opstellen van selectiecriteria.
Stel jezelf op basis van deze stap de volgende vragen:
- Zijn mijn selectiecriteria ondubbelzinnig en kunnen ze consistent worden toegepast door twee onafhankelijke reviewers?
- Heb ik alle PICO-elementen verwerkt in mijn selectiecriteria en zijn deze specifiek genoeg?
- Heb ik een duidelijke rationale gegeven voor eventuele beperkingen zoals op studietype, publicatiedatum, taal of geografische regio?
- Passen mijn selectiecriteria bij het type systematische review dat ik uitvoer (bijvoorbeeld geen secundaire studies includeren)?


Stap 6: De databanken selecteren
Je leert hoe je weloverwogen relevante databanken kiest op basis van je onderzoeksvraag, het type literatuur dat je zoekt en het onderwerp van je review. Je ontwikkelt inzicht in de sterktes en beperkingen van verschillende databanken en het belang van het zoeken in meerdere databanken bij systematische reviews.
Een systematische review vereist een transparante en reproduceerbare zoekstrategie waarbij je je ertoe verbindt om alle relevante literatuur te vinden. Dat betekent dat je in meerdere databanken moet zoeken, elk met hun eigen focus, thesaurus (bij bepaalde databanken zoals MEDLINE (via PubMed of Ovid), Embase (via embase.com) en CINAHL (via EBSCO)) en manier van indexeren. De selectie van databanken heeft een rechtstreekse impact op de volledigheid van de literatuur die je vindt.
Kies databanken op basis van:
- de inhoud van de databank (biomedisch, verpleegkundig, multidisciplinair…),
- het type bronnen (peer-reviewed artikelen, preprints, grijze literatuur, …),
- de relevantie voor je populatie, interventie of context,
- de toegang: niet alle databanken én interfaces zijn dankzij UGent/UZ Gent licenties beschikbaar.
Merk hierbij op dat een databank en interface niet hetzelfde zijn. Een databank bevat de inhoud (records en indexering), terwijl de interface bepaalt hoe je die inhoud kunt doorzoeken en welke zoekfunctionaliteiten beschikbaar zijn. Dit kan invloed hebben op hoe je zoekstrategie moet worden opgesteld en vertaald. Zo is Embase bij UGent enkel toegankelijk via de Embase.com-interface (en dus niet via Ovid) en is PsycINFO niet beschikbaar wegens geen licentie.
Voor de meeste (bio)medische onderwerpen is MEDLINE via PubMed of Ovid een logisch startpunt. Voor farmacologie is Embase vaak interessanter. We merken in de praktijk dat Embase voor bepaalde topics zorgt voor een groter aantal resultaten. Starten in Embase kan je daarom een beter overzicht geven van wat je kan verwachten. Voor verpleegkundige of paramedische onderwerpen is CINAHL sterk aanbevolen. Is je topic multidisciplinair, dan neem je best Web of Science én Scopus mee (zie hieronder bij Tip(s) en advies).
Gebruik de overzichten op de KCGG-databankenpagina om de inhoud en focus van elke databank te vergelijken. De informatiefiches (i-icoon in de kolom ‘KCGG infofiche’) geven je uitgebreide informatie over de meest gebruikte databanken aan onze faculteit.
- Kies niet automatisch alleen MEDLINE via PubMed of Ovid. Veel onderzoekers beperken zich tot één databank, vaak uit gewoonte, maar missen zo relevante studies.
- Gebruik Google Scholar niet als primaire bron. Het is geen transparante of systematische databank, maar een zoekmachine. Het is in elk geval ongeschikt om reproduceerbaar te zoeken, zoals vereist bij een systematische review.
- Combineer grote multidisciplinaire databanken (zoals Scopus en Web of Science) met vakspecifieke databanken. We raden aan om Scopus mee te nemen als je Web of Science selecteert en vice versa. Beide databanken zijn multidsciplinair, waarbij de Core Collection van Web of Science vooral is gericht op Noord-Amerika en West-Europa, terwijl Scopus verhoudingsgewijs meer publicaties aanbiedt uit groeimarkten als Azië.
- Vergeet grijze literatuur niet (zie stap 11): afhankelijk van je onderzoek kan dit hoogst relevant zijn.
- Documenteer duidelijk welke databanken je doorzocht, inclusief de interface (bijv. MEDLINE via Pubmed, Embase via Embase.com en CINAHL via EBSCO), datum en je zoekstrategie. Dit draagt bij aan de transparantie en reproduceerbaarheid van je review. Gebruik bij voorkeur de template van het KCGG om je zoekstrategie op te stellen. Je vindt een voorbeeld van een ingevulde template hier. Deze template helpt je om je concepten duidelijk te benoemen en voor elk concept een afzonderlijk zoekblok op te bouwen. Door de zoekblokken vervolgens (met cijfers) in de databank zelf te combineren (meestal met een AND-relatie), verklein je de kans op fouten met ronde haakjes die kunnen ontstaan wanneer je in Word één grote zoekblok probeert te maken.
Voor ons voorbeeld systematische review over “Zijn SSRI’s effectiever dan tricyclische antidepressiva voor de behandeling van ernstige depressieve stoornis bij adolescenten?”, zou je de volgende databanken kunnen selecteren:
- Embase (via Embase.com): belangrijk vanwege de brede dekking van medische en farmacologische literatuur. Zeker voor deze vraag die farmacologisch gericht is, een interessant startpunt.
- MEDLINE (via PubMed): voor de algemene biomedische en gezondheidsgerelateerde literatuur. Deze databank heeft een andere manier van indexeren dan bijvoorbeeld Embase en is daarom complementair.
- Cochrane Central Register of Controlled Trials (CENTRAL via Wiley): om randomised controlled trials te identificeren die mogelijk niet volledig zijn geïndexeerd in andere databanken.
- Web of Science (Core Collection via Web of Knowledge) en Scopus (via scopus.com): voor bredere interdisciplinaire dekking.
- ClinicalTrials.gov en WHO ICTRP: Om lopende of ongepubliceerde studies te identificeren en publicatiebias te minimaliseren.
- KCGG databanken-pagina. Hier vind je een overzicht van beschikbare databanken met uitleg over hun focus.
- KCGG-informatiesessies rond wetenschappelijke databanken.
- Cochrane Handbook for Systematic Reviews of Interventions – Chapter 4: Searching for and selecting studies. Dit hoofdstuk biedt uitgebreide richtlijnen voor het selecteren van bronnen.
- JBI Manual for Evidence Synthesis – Chapter 2.4.3: Developing a Search Strategy. Dit deel behandelt de selectie van databanken als onderdeel van de zoekstrategie. Beschikbaar via: https://jbi-global-wiki.refined.site/space/MANUAL
- PRISMA 2020 Statement. Hoewel een reporting guideline, beschrijft het flowdiagram en de checklist welke informatie moet worden gerapporteerd over de zoekstrategie, inclusief de gebruikte databanken. Dit kan helpen om te begrijpen wat anderen rapporteren. (www.prisma-statement.org)
Stel jezelf op basis van deze stap de volgende vragen:
- Heb ik de databanken gekozen die het meest relevant zijn voor mijn onderzoeksvraag en vakgebied?
- Heb ik een goede balans gevonden tussen algemene biomedische databanken en meer topic specifieke bronnen?
- Kan ik mijn keuze voor elke geselecteerde databank duidelijk motiveren?
- Heb ik in mijn protocol vastgelegd welke databanken ik zal doorzoeken (inclusief de zoekstrategie)?
Stap 7: Je zoekstrategie opstellen
Je leert het belang van een sensitieve zoekstrategie die is afgestemd op je onderzoeksvraag. Je leert hoe je zoektermen structureert (bijv. per concept of PICO-element). Je begrijpt het belang van een iteratief proces: test–herwerk–finaliseer.
Het ontwikkelen van een zoekstrategie is een van de belangrijkste stappen in een systematische review. Het doel is om een zo volledig mogelijk overzicht van de relevante wetenschappelijke literatuur te verkrijgen. Je zoekt niet naar een paar studies die je dankzij een eenvoudige zoekopdracht snel kunt vinden, maar naar alle studies die je onderzoeksvraag beantwoorden. Daarom moet je zoekstrategie sensitief (breed) zijn en tegelijkertijd transparant en reproduceerbaar voor anderen.
Om je zoekstrategie op te stellen, kan je de KCGG-template (en ingevuld voorbeeld van deze template) gebruiken om je concepten duidelijk te benoemen en voor elk concept een afzonderlijk zoekblok op te bouwen.
Je zoekstrategie bouw je op vanuit je onderzoeksvraag, geformuleerd met behulp van een framework zoals PICO (zie stap 4). Je zet de belangrijkste concepten uit je vraag die je het best kan definiëren en aflijnen om naar zoektermen. Deze termen bestaan uit:
- Vrije tekstwoorden: dit zijn woorden en zinsneden die voorkomen in de titel, abstract of trefwoorden van een publicatie.
- Indextermen (bij databanken waar dit van toepassing is): dit zijn gestructureerde trefwoorden uit een thesaurus van de databank, zoals MeSH (Medical Subject Headings) in PubMed, Emtree in Embase of Subject Headings in CINAHL.
Door deze twee typen zoektermen te combineren, vergroot je de kans om relevante studies te vinden. De gecontroleerde termen zorgen voor consistentie, terwijl de vrije tekstwoorden de meest recente of minder goed geïndexeerde literatuur oppikken. Je kunt meer leren over het belang van deze combinatie in onze instructievideo ‘Waarom MeSH-termen en vrije tekstwoorden combineren in je zoekstrategie’.
Om je zoektermen te verbinden en te verfijnen, gebruik je verschillende operatoren:
- Booleaanse operatoren zoals AND, OR en NOT.
- Truncatie (*) en wildcards om te zoeken naar verschillende woordvormen.
- Proximity-operatoren om aan te geven hoe dicht zoektermen bij elkaar moeten staan (van toepassing bij bepaalde databanken).
Het is aan te raden om te starten met het ontwikkelen van je zoekstrategie in één databank waar je vertrouwd mee bent, zoals MEDLINE (via PubMed) of Embase. Dit maakt het proces van experimenteren en optimaliseren efficiënter. Bekijk hier onze kennisclip voor een stappenplan om je zoekstrategie verder te optimaliseren om te bekijken of je nog relevante termen (zowel indextermen als vrije tekstwoorden) mist.
Nadat je de strategie hebt geoptimaliseerd en feedback hebt gekregen van je team, kan je de strategie finaliseren in je primaire databank. Deze versie kan je sturen naar een informatiedeskundige van het KCGG voor feedback. Wanneer je versie definitief is (na alle feedbackrondes), vertaal je de strategie naar de andere databanken die je hebt geselecteerd in stap 6 (zoals Scopus, Web of Science, CINAHL, etc.). Door deze aanpak kunnen informatiedeskundigen van het KCGG je efficiënt van feedback voorzien op één zoekstrategie. Zodra deze strategie gefinaliseerde is, kan je deze vertalen naar andere databanken. Je vindt alvast een stappenplan om je zoekstrategie te vertalen van PubMed naar Embase, WoS en Scopus in onze kennisclip hier. Een informatiedeskundige van het KCGG kan daarna de vertaalde zoekstrategie op methodologisch vlak voor je nakijken.
Verder kan je gebruik maken van ons overzicht van de syntax en operatoren voor verschillende databanken om je zoekstrategie op te stellen voor verschillende databank.
- Werk per concept of PICO-component en combineer. Neem niet alle concepten mee, dat werkt te beperkend, terwijl je je ertoe verbindt om alle bewijs te identificeren. Begin met 2 à 3 concepten en kies de concepten die je het best kan definiëren en aflijnen, waarbij je de meeste kans hebt dat ze niet op heel veel verschillende manieren in de literatuur voorkomen en waarbij de concepten gewoonlijk geïndexeerd is. Concepten zoals uitkomsten komen bijvoorbeeld vaak niet voor in titel en/of abstract en zijn mogelijk ook niet altijd geïndexeerd.
- Gebruik bij voorkeur de template van het KCGG. Je vindt een voorbeeld van een ingevulde template hier. Deze template helpt je om je concepten duidelijk te benoemen en voor elk concept een afzonderlijk zoekblok op te bouwen. Door de zoekblokken vervolgens (met cijfers) in de databank zelf te combineren (meestal met een AND-relatie), verklein je de kans op fouten met ronde haakjes die kunnen ontstaan wanneer je in Word één grote zoekblok probeert te maken.
- Zoek niet enkel op vrije tekstwoorden of indextermen, combineer beide. Als je een indexterm meeneemt, neem deze dan ook mee als vrije tekstwoord en vice versa.
- Je kan inspiratie vinden in zoekstrategieën van andere systematische reviews (eventueel geïdentificeerd in stap 1) of zoekfilters. Zie onze website ‘Waar vind ik systematische reviews?’ en ‘Wat zijn zoekfilters en waar vind ik die?’.
- Zorg dat je voldoende synoniemen en varianten opneemt. Let wel dat je geen overbodige termen meeneemt. Als je “depressive disorder” als vrije tekstwoord meehebt, dan hoef je “major depressive disorder” niet apart mee te nemen. De resultaten van het laatste zullen al verwerkt zitten in de resultaten van “depressive disorder”.
- Documenteer je volledige zoekstrategie en keuzes zoals beperkingen (bijv. op taal of datum) tijdens het opstellen. Zorg dat je deze keuzes steeds transparant vermeldt en voldoende motiveert. Zoals aangegeven in de rapporteringsrichtlijnen van PRISMA 2020, dien je de volledige zoekstrategie voor alle databanken, registers en websites te rapporteren en vermelden of er filters of beperkingen zijn toegepast.
- Start niet te snel met vertalen naar een andere databank zonder een gefinaliseerde zoekstrategie te hebben.
- Het KCGG kan indien gewenst je zoekstrategie op methodologisch vlak nakijken en suggesties maken. Het blijft echter de eindverantwoordelijkheid van de student of onderzoeker om de optimalisatiestappen uit te voeren en dankzij de evaluatie van de literatuur de meest geschikte zoektermen op te nemen.
Een overzicht van beschikbare tools om je zoekstrategie op te bouwen of bijkomende termen te identificeren vind je via de ‘Library of Search Strategy Resources’.
- KCGG databanken-pagina. Hier vind je een overzicht van beschikbare databanken met links naar informatiefiches en sessies die je uitgebreid informatie geven over het opstellen van een zoekstrategie in de databank.
- KCGG-informatiesessies rond wetenschappelijke databanken.
- Cochrane Handbook for Systematic Reviews of Interventions – Chapter 4: Searching for and selecting studies. Dit hoofdstuk (vanaf 4 Designing search strategies) biedt uitgebreide richtlijnen voor het opstellen van je zoekstrategie.
- JBI Manual for Evidence Synthesis – Chapter 2.4.3: Developing a Search Strategy. Dit deel behandelt de het opstellen van een zoekstrategie. Beschikbaar via: https://jbi-global-wiki.refined.site/space/MANUAL
- KCGG template (en voorbeeld van template) voor het opstellen van je zoekstrategie. Deze template helpt je om je concepten duidelijk te benoemen en voor elk concept een afzonderlijk zoekblok op te bouwen.
De PRESS-checklist is een ideaal hulpmiddel om na te gaan of je zoekstrategie volledig en kwalitatief is uitgewerkt. Deze checklist helpt je te controleren of alle relevante elementen zijn meegenomen zoals correcte terminologie, juiste combinatie van zoektermen en passende gebruik van booleaanse operatoren. Als je zoekstrategie is gefinaliseerd, kan een informatiedeskundige van het KCGG de PRESS-checklist voor jou aanvullen.
Naast zelfevaluatie, kan je ook feedback vragen voor je zoekstrategie aan een KCGG-informatiedeskundige. Vul daarvoor ons formulier in en gebruik bij voorkeur de template van het KCGG. Je vindt een voorbeeld van een ingevulde template hier. Deze template helpt je om je concepten duidelijk te benoemen en voor elk concept een afzonderlijk zoekblok op te bouwen. Door de zoekblokken vervolgens (met cijfers) in de databank zelf te combineren (meestal met een AND-relatie), verklein je de kans op fouten met ronde haakjes die kunnen ontstaan wanneer je in Word één grote zoekblok probeert te maken.


Stap 8: je protocol registreren (en publiceren)
In deze stap leer je waar en hoe je een protocol kan registreren of publiceren.
Een protocol is het “plan” voor je review. Dit protocol heb je eerder al beginnen opstellen bij stap 3. Het omvat je onderzoeksvraag en doelstelling, je inclusie- en exclusiecriteria, je zoekstrategie*, je selectieprocedure, je data-extractieplan, je kwaliteits- of biasbeoordeling, je analyse- en syntheseplan, je tijdslijn en de rolverdeling. Volg voor het opstellen de PRISMA-P richtlijnen, die aangeven welke onderwerpen minimaal in je protocol dienen opgenomen te worden en op welke manier. Het beschikbaar stellen van je protocol zorgt voor transparantie, voorkomt onbedoelde duplicatie en helpt bias te verminderen.
* Het is gebruikelijk om de zoekstrategie pas te delen bij publicatie van je review.
Zorg dat alle relevante teamleden (bijv. promotor, begeleider, 2de reviewer, ev. statisticus, ev. Informatiedeskundige KCGG) betrokken zijn bij het opstellen van het protocol en vraag actief om hun feedback. Als je feedback wenst voor je protocol van een informatiedeskundige van het KCGG, dan kan je dit vragen via ons formulier.
Finaliseer en registreer je protocol (zie ‘Tools en platforms’) bij voorkeur na je verkennende zoekopdracht, maar ten laatste voordat je start aan je data-extractie.
PROSPERO is een internationaal register voor systematische reviews dat transparantie bevordert en duplicatie van onderzoek helpt voorkomen. Vraag je registratienummer van je protocol in PROSPERO aan en voeg er ook de PDF van je protocol toe. Als je review géén uitkomst heeft die gerelateerd is aan de menselijke gezondheid (bijv. sportprestaties of adoptie)? In dat geval kan je je protocol wel registeren via het Open Science Framework (OSF). Registeren kan zowel bij PROSPERO als bij OSF gratis.
Wie internationale peer review wil, kan er daarnaast voor kiezen om het protocol te publiceren. Tijdschriften zoals Systematic Reviews of BMJ Open aanvaarden dit type publicatie. Let op: deze Open Access-tijdschriften vragen een publicatiekost.
Rammant, E. et al. Rehabilitation interventions to improve patient-reported outcomes and physical fitness in survivors of muscle invasive bladder cancer: a systematic review protocol. Protocol gepubliceerd in BMJ open (doi.org/10.1136/bmjopen-2017-016054) en geregisreerd op PROSPERO: https://www.crd.york.ac.uk/PROSPERO/view/CRD42017055306
- PRISMA-P checklist (Preferred Reporting Items for Systematic Review and Meta-Analysis Protocols) bevat aanbevolen items voor een systematisch reviewprotocol
- Cochrane Handbook for Systematic Reviews of Interventions – Chapter 1 – Sectie 1.5: Protocol development
Stel jezelf op basis van deze stap de volgende vragen:
- Heb ik het meest geschikte platform voor registratie gekozen?
- Zijn er financiële middelen ter beschikking in het geval je wenst te publiceren (de UGent biedt geen steun bij APCs)
- Heb ik alle onderwerpen van de PRISMA-P checklist opgenomen in mijn protocol?
Stap 9: je literatuuronderzoek in de databanken uitvoeren en deduplicatie
Je leert hoe je een zorgvuldig gecreëerde en gefinaliseerde zoekstrategieën daadwerkelijk uitvoert in de geselecteerde databanken (zie stap 6). Je leert hoe je alle zoekacties nauwkeurig registreert, de resultaten exporteert naar een referentiemanagementtool en de verzamelde literatuur dedupliceert.
Het uitvoeren van je zoekstrategie is de concrete implementatie van het voorbereidende werk dat je tot nu hebt gedaan. Deze stap moet transparant en reproduceerbaar zijn. Dit betekent dat iemand anders, door jouw beschrijving te volgen, precies dezelfde zoekacties zou moeten kunnen uitvoeren en tot dezelfde resultaten zou moeten komen.
De belangrijkste fases van deze stap zijn:
- Gebruik gefinaliseerde zoekstrategieën: voer exact voor elke specifieke databank de zoekstrategie uit die je in de vorige stappen hebt ontwikkeld en na feedback hebt gefinaliseerd en vertaald naar verschillende databanken.
- Exporteer alle resultaten op 1 dag en registreer de zoekdatum: voor elke zoekopdracht in de databank is het van belang om de exacte datum te noteren. Dit is niet alleen een vereiste voor de PRISMA-richtlijnen, maar ook belangrijk voor de transparantie. Het toont aan tot welke datum je de literatuur hebt meegenomen en zorgt voor reproduceerbaarheid. Ook voor die reden voer je bij voorkeur alle zoekopdrachten voor de verschillende databanken uit op 1 dag.
- Exporteer de resultaten: nadat je de zoekopdrachten hebt uitgevoerd, exporteer je alle gevonden resultaten. Gebruik hiervoor een geschikt bestandsformaat, zoals een RIS-bestand dat gemakkelijk kan worden geïmporteerd in referentiemanagementsoftware zoals EndNote of Zotero. De RIS bestanden en library zijn ook nuttig om je PRISMA flowchart op te stellen (zie stap 11)
- Deduplicatie: gevonden literatuur uit meerdere databanken zal onvermijdelijk overlappingen bevatten. De volgende stap is het verwijderen van deze dubbele artikels. Deduplicatie is van belang om te voorkomen dat jij en je teamleden dubbel werk moeten doen tijdens de selectieprocedure (zie stap 10) en om de efficiëntie van je review te waarborgen. Deduplicatie kan in Endnote (zie onze onderzoektip hier) of met tools zoals DedupEndNote of in een screeningtool zoals Rayyan.
- Wees nauwkeurig en methodisch. Voer de zoekstrategieën in de databanken met uiterste precisie uit, exact zoals je ze had gefinaliseerd. Fouten kunnen leiden tot het missen van belangrijke studies.
- Exporteer zorgvuldig. Zorg ervoor dat je alle relevante velden exporteert (zoals titel, abstract, auteurs en publicatiejaar) in een format dat je kan importeren in de tools die je zal gebruiken. Dit is nodig voor de latere selectie (zie stap 10) en data-extractie (zie stap 13). Controleer na het exporteren of alle records correct zijn overgebracht.
- Dedupliceer met de nodige zorg. Referentiemanagementtools zoals EndNote hebben ingebouwde deduplicatiefuncties (zie onze onderzoektip hier). Gebruik deze, maar wees ervan bewust dat deze automatische functies soms records missen die niet exact overeenkomen (bv. kleine verschillen in auteursnamen). Tools zoals DedupEndNote zorgen vaak voor betere resultaten hierin door de metadata eerst gelijk af te stemmen.
- Houd een logboek bij. Naast de zoekdatum is het nuttig om een gedetailleerd logboek bij te houden van al je zoekacties, inclusief de gebruikte databanken, de datum, de zoekstrategie en het aantal gevonden resultaten. Dit helpt bij de rapportage en het invullen van het PRISMA-flowdiagram.
- Houd een overzicht bij van de versies van de software die je gebruikt heb. Dit zal je nodig hebben voor een correct verwijzing naar de tools in je manuscript of thesis. Bijv. Rayyan: https://www.rayyan.ai/cite/?_ga=2.259374409.2136298842.1757424699-345423004.1696848704
- Referentiemanagementsoftware zoals EndNote (campuslicentie via UGent, gratis te installeren voor studenten en onderzoekers via Academic Software) om je referenties bij te houden en te dedupliceren.
- DedupEndNote is een tool om je EndNote RIS-bestanden te dedupliceren. Je krijgt een nieuw RIS-bestand met de unieke records, dat kan worden geïmporteerd in EndNote of in Rayyan.
- Review software zoals Rayyan. Rayyan is een online tool die specifiek is ontworpen om het selectieproces te versnellen en deduplicatie te vereenvoudigen.
- KCGG-informatiesessies rond EndNote en individuele sessies rond de databanken tonen je hoe je resultaten kan exporteren en importeren.
- Onderzoektip ‘EndNote: dubbele referenties verwijderen’ https://onderzoektips.ugent.be/nl/tips/00001021/ . Hier vind je stapsgewijze handleidingen voor het dedupliceren in EndNote.
Stel jezelf de volgende vragen:
- Heb ik de gefinaliseerde zoekstrategieën zonder fouten uitgevoerd in elke databank?
- Heb ik de exacte datum en aantal resultaten van elke zoekopdracht in elke databank genoteerd?
- Zijn alle resultaten correct geëxporteerd en geïmporteerd in mijn referentiemanagementsoftware?
- Heb ik zoveel als mogelijk duplicaten verwijderd?
- Kan ik op basis van mijn notities een PRISMA-flowdiagram (zie stap 12) opstellen dat mijn proces nauwkeurig weergeeft?


Stap 10: Studieselectie
Het proces van studieselectie omvat het zorgvuldig toepassen van de vooraf gedefinieerde selectiecriteria uit het protocol, met als doel de studies te selecteren die inhoudelijk bijdragen aan de beantwoording van de onderzoeksvraag en dus relevant zijn voor de systematische review.
Deze stap volgt direct op de deduplicatie en wordt uitgevoerd in twee fasen: 1) de screening van alle titels en abstracten en 2) de evaluatie van de volledige tekst van potentieel relevante studies. Tijdens de 1ste fase worden irrelevante records uitgesloten en worden potentieel relevante records doorgeschoven voor full tekst evaluatie. Tijdens die tweede fase wordt de reden van exclusie vastgelegd om de transparantie van het selectieproces te waarborgen.
Bij voorkeur voeren minstens twee reviewers deze stap uit om bias te beperken. Volgens Cochrane-richtlijnen moet minimaal de volledige tekstevaluatie door twee onafhankelijke beoordelaars gebeuren. In de praktijk is het echter ook heel gebruikelijk dat beide beoordelaars ook afzonderlijk de titels en abstracten beoordelen. Zelfs met heel duidelijk gedefinieerde selectiecriteria is het nog steeds mogelijk dat er fouten gemaakt worden of dat de beoordeling verschillend is (owv verschil of gebrek aan inhoudelijke of methodologische kennis). Bij verschil van mening proberen de reviewers consensus te bereiken, of er wordt een derde reviewer ingeschakeld. Dit gebeurt volgens de procedure zoals beschreven in je protocol.
Bij twijfel tijdens de screening van titel en abstract (bijvoorbeeld bij onvoldoende informatie) wordt het artikel doorgestuurd naar de volledige tekstevaluatie. Een studie wordt alleen uitgesloten als er een duidelijke reden voor exclusie is.
Tijdens de volledige tekstevaluatie is het raadzaam een hiërarchie op te stellen voor de redenen van exclusie. Zo kun je duidelijk aangeven hoeveel studies om welke reden zijn uitgesloten.
Indien de full tekst niet beschikbaar is dankzij het U(Z)Gent netwerk, ga dan na of er een open access-versie beschikbaar is via Google Scholar.
Het is aan te raden om de screening eerst te testen voordat de volledige dataset wordt beoordeeld. Dit helpt om de selectiecriteria te verifiëren, eventuele onduidelijkheden op te sporen en ervoor te zorgen dat alle reviewers de criteria op een consistente manier toepassen. Zo wordt de betrouwbaarheid en reproduceerbaarheid van de systematische review vergroot.
Rayyan.ai biedt een gratis functionaliteit die het proces van studieselectie kan ondersteunen. Beoordelaars kunnen geblindeerd screenen, waardoor hun beoordelingen onafhankelijk blijven. Daarnaast kunnen relevante sleuteltermen worden gemarkeerd en gefilterd, wat het overzicht vergemakkelijkt en het selectieproces efficiënter maakt. Dit draagt bij aan een systematische en reproduceerbare beoordeling van de literatuur.
DistillerSR is een webgebaseerde tool waarmee je naast studieselectie – inclusief de voordelen zoals vermeld bij Rayyan – ook data-extractie en kwaliteitsbeoordeling kunt uitvoeren. De tool is niet gratis, maar via een licentie van het KCGG kun je een project aanvragen. Voor meer informatie kun je contact opnemen met het KCGG.
Stap 11: zoeken naar grijze literatuur en citation tracking
Je leert wat grijze literatuur is en waar je grijze literatuur kan vinden. Bovendien leer je wat citation tracking is, waarom het nuttig is en hoe je dit kan doen.
De term ‘grijze literatuur’ wordt vaak gebruikt om te verwijzen naar rapporten – zowel geprint als online beschikbaar – die buiten de traditionele commerciële uitgeverijen worden gepubliceerd. Voorbeelden zijn thesissen (master of PhD), bijdragen aan congressen, overheidsrapporten, preprints, ongoing clinical trial data, …
Volgens het Cochrane handboek is het ‘highly desirable’ om naar grijze literatuur te zoeken. De zoektocht naar grijze literatuur moeten zo uitgebreid mogelijk zijn om het risico op publicatiebias te verminderen en om zoveel mogelijk relevante evidence te identificeren.
De term ‘citation tracking’ …
Hou in je logboek bij welke bronnen van grijze literatuur je doorzocht hebt, wie de zoektocht gedaan heeft (bij voorkeur met 2 personen onafhankelijk), welke zoektrategie (of trefwoorden) je gebruikt hebt, hoeveel resultaten je gescreend hebt en hoeveel grijze literatuur je finaal geïncludeerd hebt.
Sommige databanken bevatten naar tijdschriftartikelen (gepubliceerd door commerciële uitgeverijen) ook grijze literatuur. Zo bevat de Web of Science Core Collection en Embase congresmateriaal, terwijl PsycINFO en CINAHL enkele thesissen bevatten. Omdat gezondheidsgerelateerde bibliotheekdatabases doorgaans geen volledige dekking van grijze literatuur bieden, moeten ook andere bronnen worden doorzocht om literatuur te identificeren die niet formeel is gepubliceerd.
Geen enkele bron is volledig, maar de keuze dient gepast te zijn om te verantwoorden dat men het maximale gedaan heeft.
Link naar PRISMA flowchart (stap 12)?

Stap 12: PRISMA-flowchart opmaken
Je leert hoe je het selectieproces van je studies visualiseert en rapporteert met behulp van het PRISMA-flowchart. Dit diagram is een onderdeel van elke systematische review, omdat het de transparantie en reproduceerbaarheid van je selectieprocedure aantoont.
Het PRISMA-flowchart (Preferred Reporting Items for Systematic Reviews and Meta-Analyses) is een gestandaardiseerd diagram dat de weg van elke potentiële studie volgt, vanaf het initiële zoeken in databanken tot de uiteindelijke exclusie of inclusie in je review. Het documenteert elke stap in het selectieproces en verklaart waarom bepaalde studies zijn uitgesloten. Het invullen van deze flowchart zorgt ervoor dat je de methodologie van je review kan valideren en dat je lezers voorziet van een duidelijk en traceerbaar overzicht van de studies.
Het opstellen van deze flowchart is de visuele samenvatting van de selectieprocedure die je in de voorgaande stappen hebt doorlopen. Het maakt je keuzes transparant en helpt lezers om de scope en beperkingen van je review te begrijpen.
Let erop dat de PRISMA-richtlijnen verschillen van de PRISMA-flowchart. Beide zijn belangrijk en hebben verschillende doeleinden voor het rapporteren van je systematische review. De PRISMA-richtlijnen zijn een bredere set aanbevelingen, waaronder een gedetailleerde checklist en richtlijnen voor het rapporteren van de methodologie van systematische reviews, wat zorgt voor transparantie en methodologische transparantie. De PRISMA-flowchart is een visueel diagram dat het proces van artikelselectie in een systematische review weergeeft, inclusief het aantal documenten dat in verschillende fasen wordt gevonden, gescreend en uiteindelijk opgenomen.
De PRISA-flowchart voor je review kan je opmaken via de tool PRISMA Flow Diagram: https://estech.shinyapps.io/prisma_flowdiagram/.
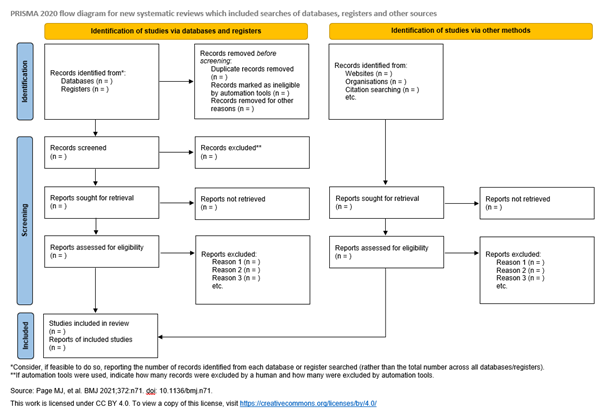
Page MJ, McKenzie JE, Bossuyt PM, Boutron I, Hoffmann TC, Mulrow CD, et al. The PRISMA 2020 statement: an updated guideline for reporting systematic reviews. BMJ 2021;372:n71. doi: 10.1136/bmj.n71. http://www.prisma-statement.org/
Informatie rond het opstellen van de PRISMA-flowchart vind je op de PRISMA-statement website.
Stel jezelf de volgende vragen:
- Heb ik alle aantallen van mijn zoek- en selectieproces nauwkeurig genoteerd?
- Kan ik voor elke uitgesloten studie (na full text evaluatie) een specifieke en duidelijke reden geven?
- Is het uiteindelijke PRISMA-flowchart logisch en kan een externe lezer mijn selectieproces volledig volgen?
- Zijn de aantallen in mijn flowchart consistent met de aantallen in mijn logboek en die van mijn referentiemanagementtool?
De stappen 13 tem. 18 zijn momenteel nog in opbouw.
